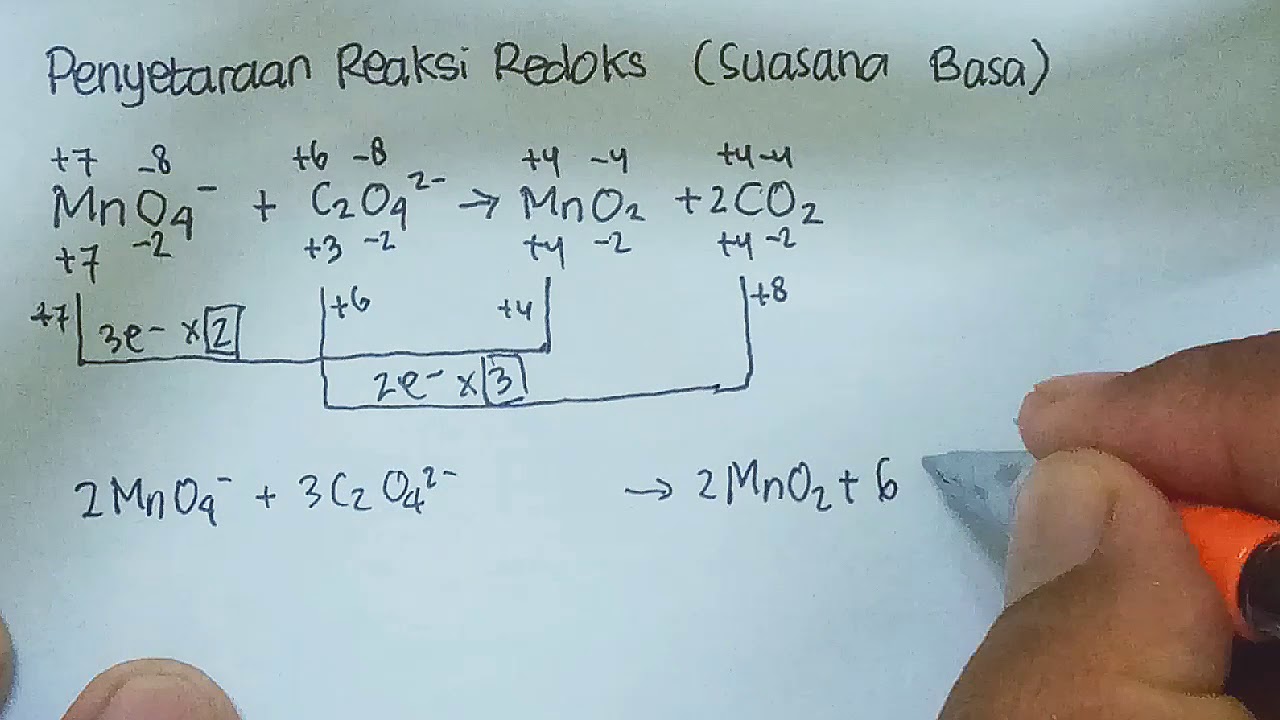
Setarakan Reaksi Redoks Berikut Dengan Cara Bilangan Oksidasi Mno4 So3. 14 penyetaraan reaksi redoks ada 2 metode yg lebih eksak untuk menyetarakan suatu reaksi redoks yaitu metode setengah reaksi dan metode bilangan oksidasi adapun pedoman penyetaraan reaksi redoks sebagai berikut. Menyetarakan perubahan bilangan oksidasi itu dengan cara memberikan koefisien reaksi yang sesuai.
Bilangan oksidasi biloks unsur o dalam h2o koh h2so4 dan na3po4 bernilai 2. Pada reaksi ini atom zn dan n. A dlm suasana asam b dlm suasana basa pihak yg kurang o ditambah h2o sebanyak kekurangannya kemudian pihak yg lain ditambah.
Bagi reaksi menjadi 2 satu reduksi dan satu oksidasi.
Cara penyetaraan reaksi redoks dengan sistem setengah reaksi dilakukan dengan tahapan tahapan sebagai berikut. Menyetarakan reaksi redoks dengan cara perubahan bilangan oksidasi pbo menerapkan konsep reaksi oksidasi reduksi dan elektrokimia dalam teknologi dan kehidupan sehari hari. Samakan jumlah atom o dengan menambahkan h 2 o di yang kurang o sebanyak kekurangannya suasana asam atau menambahkan h 2 o di yang lebih o sebanyak kelebihannya suasana basa. Jumlah suatu bilangan oksidasi unsur unsur dalam senyawa ialah 0 nol.
